Los bebés nacen con un sistema inmunitario inmaduro. Hasta ahora, se creía que el parto era la primera ocasión que tenían los microorganismos de la madre de colonizar el intestino del bebé y por tanto, modular el sistema inmunitario.
Pero un equipo compuesto por científicos suizos y alemanes acaba de descubrir que este proceso de moldeado del sistema inmunitario comienza durante el embarazo, es decir mucho antes de lo que se pensaba.
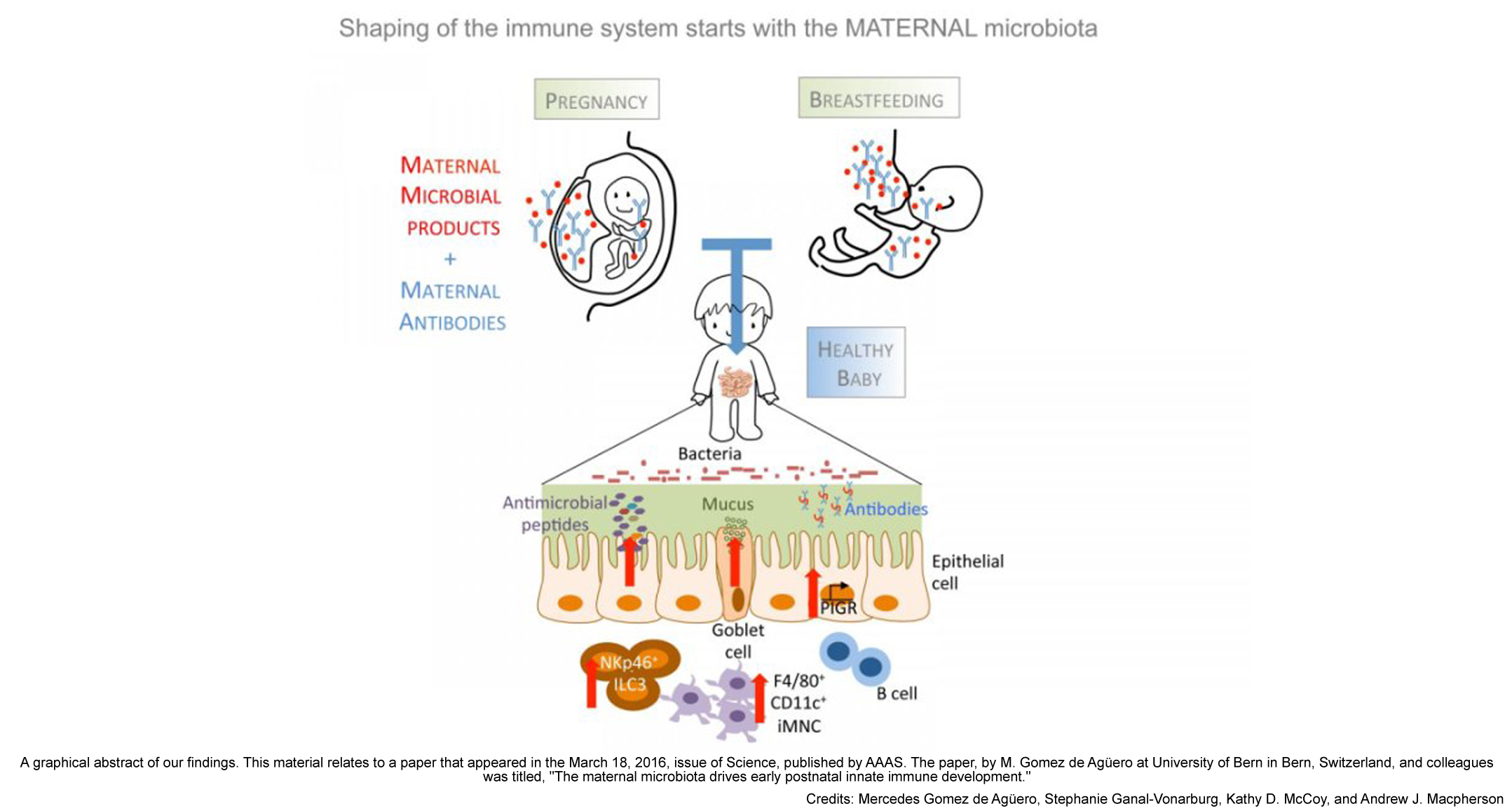
Según sus hallazgos, publicados en la revista Science, ciertas moléculas producidas por la microbiota intestinal y fragmentos bacterianos no vivos son transferidos de la madre al niño a través de la placenta o, más adelante, mediante los anticuerpos presentes en la leche materna. Tanto moléculas como fragmentos podrían estimular las células inmunitarias del recién nacido para prepararlo a combatir los microorganismos presentes en su propio intestino.
A fin de demostrar esta teoría, los investigadores llevaron a cabo un estudio con roedores: criaron ratones desprovistos de gérmenes y una vez preñados, los colonizaron temporalmente con una variante de E. coli diseñada para desaparecer con el tiempo y así conseguir que la madre estuviera de nuevo desprovista de gérmenes en el momento del alumbramiento.
Los investigadores constataron sorprendidos que esta colonización de la madre con E. coli afectaba al sistema inmunitario de la cría. En efecto, después del parto, en los intestinos de los bebés nacidos de madres colonizadas encontraron un mayor número de ciertas células inmunitarias (como las células linfoides y mononucleares) que en los de los nacidos de madres completamente desprovistas de gérmenes. Y esas células inmunitarias seguían presentes incluso tras el destete.
«Hemos constatado que durante el embarazo, pequeños fragmentos sin vida de bacterias del intestino de la madre pasaban de la placenta al feto para comenzar a formar el sistema inmunitario de la cría», explica Mercedes Gómez de Agüero, investigadora de la Universidad de Berna (Suiza) y autora principal del estudio, en una entrevista concedida a Gut Microbiota for Health.
«No hemos hallado bacterias [vivas], [ni] en la placenta [ni] en el feto. Nuestra investigación [muestra] que la colonización con bacterias vivas comienza tras el nacimiento», puntualiza la científica.
De hecho, esas moléculas inertes a las que se refiere Gómez de Agüero preparan a la cría para la colonización bacteriana tras el parto. La investigadora observó un incremento de células en el sistema inmunitario del bebé y una activación de la expresión génica implicada en la formación de la barrera intestinal, responsable de la contención de la microbiota en el interior del intestino.
Por otra parte, los grupos de animales presentaban diferentes modelos de expresión génica en sus intestinos. Comparadas con las crías nacidas de madres desprovistas de gérmenes, las crías expuestas a microbios en el útero tenían una expresión mayor de numerosos genes, como los que influyen en la división y la diferenciación celulares, el metabolismo y por supuesto, la función inmunitaria.
¿Pero por qué comienza este proceso de influencia microbiana durante la gestación? Los autores sugieren en su artículo que esta influencia microbiana en las crías durante el embarazo podría tener un papel clave en la preparación del sistema inmunitario para la exposición a la gran variedad de microbios que se alojarán en su intestino a lo largo de su vida.
«A raíz de esto, el recién nacido será capaz de controlar las bacterias de sus intestinos y su sistema inmunitario podrá responder de forma atenuada y proporcionada a la presencia de moléculas bacterianas en sus órganos», añade Gómez de Agüero en un correo electrónico dirigido a Gut Microbiota for Health. «Esta preparación del sistema inmunitario del recién nacido durante el embarazo es la que le permite desarrollar una respuesta adecuada a la colonización bacteriana sin reaccionar desproporcionadamente ni infectarse».
De hecho, los investigadores comprobaron que los sistemas inmunitarios de las crías nacidas de madres colonizadas durante el embarazo también parecían protegerlas contra la inflamación y las infecciones bacterianas. «Averiguar cuándo comienza a prepararse el sistema inmunitario del bebé podría contribuir a la mejora de esa preparación y así prevenir enfermedades infantiles», concluye Gómez de Agüero.
Este experimento demuestra asimismo que la transferencia microbiana también se lleva a cabo a través de la leche materna, ya que en los ratones nacidos de madres desprovistas de gérmenes y alimentados con leche de madres colonizadas se produjo un incremento de ciertas células inmunitarias.
Si bien estos hallazgos se basan en modelos animales, podrían aportar nuevas pistas acerca del desarrollo inicial del sistema inmunitario en los humanos. El estudio revela el mecanismo por el que la microbiota materna podría ejercer su poderoso efecto sobre el desarrollo de la cría durante el embarazo.
Referencias:
Mercedes Gómez De Agüero, Stephanie C. Ganal-Vonarburg, Tobias Fuhrer, et al. The maternal microbiota drives early postnatal innate immune development. Science, 2016DOI: 1126/science.aad2571